“Mijn bloedwaarden zijn goed, zegt de huisarts. Maar ik voel me niet goed.”
Een zin die ik regelmatig hoor. En precies hier wordt het voor mij interessant, want er zijn bloedwaarden die zelden standaard worden geprikt, maar die wél veel vertellen over hoe je lichaam écht functioneert. Homocysteïne is daar een goed voorbeeld van.
Homocysteïne is geen “enge stof”, het is een normaal tussenproduct uit je eiwitstofwisseling. Maar als de recycling ervan niet lekker loopt, stapelt het zich op. En juist dat stapelen is interessant, omdat het iets zegt over twee kwetsbare systemen: je bloedvaten én je brein.
1. Wat is homocysteïne precies?
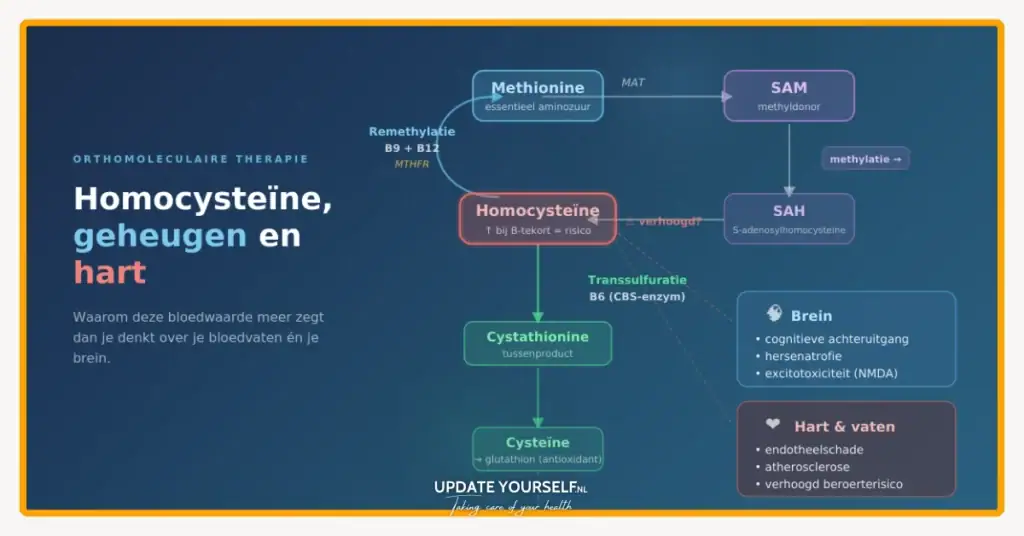
Je lichaam maakt homocysteïne aan wanneer het methionine (een aminozuur uit eiwitten) verwerkt. Normaal gesproken wordt homocysteïne daarna snel weer “doorgegeven” in de biochemie:
- óf terug naar methionine (via methylatie),
- óf door naar cysteïne (via transsulfuratie).
Voor beide routes zijn vooral folaat (vitamine B11/B9), vitamine B12 en vitamine B6 nodig. Als één van die schakels hapert, kan de spiegel stijgen.
Praktisch voorbeeld: Vergelijk het met een lopende band in een fabriek. Zolang alle medewerkers (B-vitaminen) op hun plek staan, loopt alles door. Valt er één uit, dan stapelen de producten (homocysteïne) zich op.
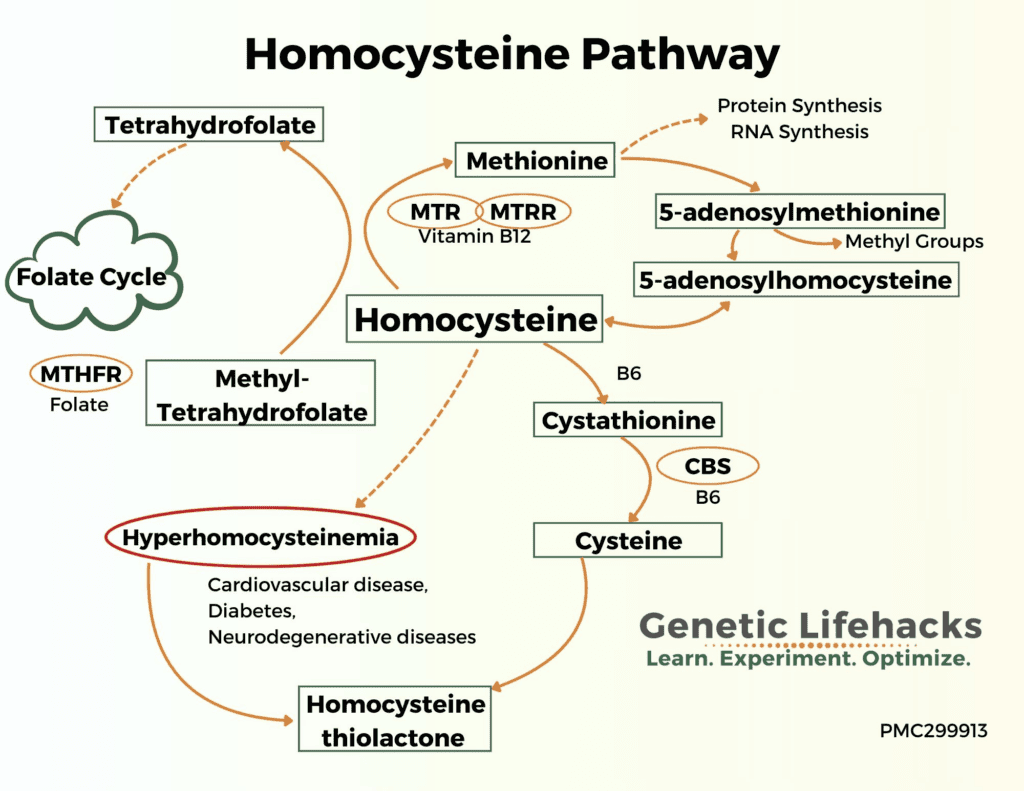
2. Waarom een verhoogde waarde je brein kan schaden
Een verhoogd homocysteïne wordt al jaren gekoppeld aan snellere cognitieve achteruitgang en een hoger risico op dementie, waaronder Alzheimer en vasculaire dementie [1][2][4].
De mechanismen die hierbij spelen:
Snellere krimp van hersenweefsel bij kwetsbaarheid
In de VITACOG-studie (bij mensen met milde cognitieve achteruitgang) liet behandeling met foliumzuur, B12 en B6 een significant langzamere hersenatrofie zien dan placebo [2]. Belangrijk: dit effect was het sterkst bij deelnemers met een hoge uitgangswaarde van homocysteïne én een goede omega-3 status [11][12].
Meer druk op zenuwcellen
Homocysteïne kan zenuwcellen belasten via excitotoxiciteit (overprikkeling van glutamaatreceptoren, met name NMDA-receptoren) [5].
Oxidatieve stress en ontstekingsactivatie
Hogere spiegels worden in verband gebracht met meer oxidatieve stress, ontstekingsactivatie en verstoring van barrièresystemen in de hersenen [3][4].
Praktisch voorbeeld: Een recente studie (2024) liet zien dat verhoogd homocysteïne zelfs versnelde epigenetische veroudering veroorzaakt bij mensen met milde cognitieve achteruitgang. Je cellen “verouderen” letterlijk sneller [13].
3. Waarom homocysteïne óók een cardiovasculair signaal is
Homocysteïne is niet alleen een “brein-marker”. Het is ook gelinkt aan vaatrisico, zoals atherosclerose (slagaderverkalking) en beroerte, mede omdat het endotheel (de binnenwand van bloedvaten) kan verstoren en de vaatfunctie onder druk kan zetten [6][14].
Een grote Mendeliaanse randomisatiestudie (2021) bevestigde dat genetisch verhoogd homocysteïne causaal samenhangt met een hoger risico op beroerte, met name ischemische beroerte en subarachnoïdale bloeding [15].
Belangrijke nuance (die vaak wordt overgeslagen)
B-vitaminen verlagen homocysteïne betrouwbaar, maar in grote cardiovasculaire trials vertaalt dat zich niet consequent naar minder hartinfarcten of “grote” cardiovasculaire events. In de HOPE-2 studie was er wél een lagere beroertekans, maar geen daling in het samengestelde eindpunt [6].
In NORVIT (na een hartinfarct) werd geen voordeel gezien en werden er zelfs signalen gevonden die tegen routinematig hooggedoseerd suppleren pleiten in die setting [7].
Een recente review (2025) concludeert dat homocysteïne vooral waardevol is als risico-marker en metabool signaal, niet als blind doelwit om alleen maar omlaag te drukken [14]. Dat sluit aan bij hoe ik het in de praktijk inzet: eerst begrijpen waarom het verhoogd is, dan gericht corrigeren.
4. Welke waarde is “te hoog”?
De referentiewaarden variëren per context:
- Veel labs hanteren 5–15 µmol/L als referentiegebied.
- In de huisartsgeneeskundige literatuur wordt >15 µmol/L vaak als verhoogd gezien [1].
- In preventie- en breinliteratuur kom je vaak een streefwaarde <10 µmol/L tegen, zeker bij mensen met cognitieve risico’s of klachten [3].
Praktisch: “Normaal” op een labformulier betekent niet altijd “optimaal”. Bij iemand met vermoeidheid, concentratieklachten of cardiovasculaire risicofactoren kijk ik kritischer naar waarden boven de 10.
5. Waarom stijgt homocysteïne?
De top 7 die ik in de praktijk het vaakst tegenkom:
- B12-tekort of suboptimale B12-status – ook bij “normale” serum B12 kan functioneel tekort spelen.
- Lage folaatstatus – door voeding, opname of hogere behoefte.
- B6-status onvoldoende – let op: te hoog doseren is ook niet de bedoeling (zie stap 3).
- Nierfunctie – homocysteïne kan stijgen bij verminderde klaring.
- Schildklier – hypothyreoïdie (trage schildklier) kan bijdragen.
- Leefstijl – roken, hoge alcoholinname, weinig beweging.
- Genetische varianten zoals MTHFR – met name relevant bij lage folaatstatus. Het MTHFR 677C→T polymorfisme kan ervoor zorgen dat folaat minder efficiënt wordt omgezet, waardoor homocysteïne sneller stijgt [14][15].
6. Wat kun je doen als je waarde verhoogd is?
Stap 1: Slim meten (niet alleen homocysteïne)
Laat bij voorkeur in één ronde meenemen (afhankelijk van je situatie):
- Homocysteïne
- Vitamine B12-status (bij voorkeur met functionele interpretatie; arts/therapeut/lab kan hierin sturen)
- Folaat (actieve vormen, geen synthetisch foliumzuur!)
- Vitamine B6 (waar relevant, actieve vormen, geen pyridoxine)
- Nierfunctie (creatinine/eGFR)
- Schildklier (TSH, eventueel FT4)
- Groot bloedbeeld met differentiatie
Praktisch: Bij een verhoogde waarde wil je weten: is dit vooral tekort, opname/gebruik, nier/schildklier, of een combinatie?
Stap 2: Voeding als basis (meestal de grootste winst)
- Dagelijks bladgroenten (folaat).
- Peulvruchten en volkoren (folaat, B6).
- Eieren, vis, vlees of zuivel (B12, afhankelijk van je eetpatroon).
- Consistent eten, niet “af en toe een gezonde dag”.
Stap 3: Gerichte suppletie (alleen als het past)
De meest gebruikte combinatie is: folaat + B12 + B6 (en soms B2/riboflavine). In trials verlaagt dit homocysteïne aantoonbaar [2][6].
Twee praktische aandachtspunten die wél belangrijk zijn:
- Start je met foliumzuur/folaat in actieve vormen, sluit dan een B12-tekort uit of behandel dat mee. Foliumzuur kan bloedarmoede maskeren terwijl neurologische B12-problematiek kan doorsluimeren [8].
- B6 is nuttig, maar langdurig hoog doseren kan neuropathie (zenuwschade) geven. In Nederland is er een wettelijke bovengrens voor B6 in supplementen ingesteld [9].
Interessant: Er zijn aanwijzingen dat omega-3 vetzuren en B-vitaminen synergetisch werken. Een studie liet zien dat de combinatie van vitamine B12 en visolie homocysteïne met 39% verlaagde, versus 22% met B12 alleen [12]. In de VITACOG-studie was het beschermende effect op hersenatrofie ook het sterkst bij deelnemers met een goede omega-3 status [2][11]. Dit past bij wat we al weten over het belang van omega-3 voor het zenuwstelsel (lees ook mijn artikel over ADHD en omega-3).
Stap 4: Leefstijl die écht meetelt
- Stoppen met roken en alcohol matigen (als dit speelt).
- Bewegen (regelmatig, niet perfect).
- Slaap/stress: niet “zweverig”, maar omdat methylatie- en herstelprocessen hier direct last van kunnen hebben bij chronische druk.
Kort gezegd
Homocysteïne is zo interessant omdat het relatief goedkoop te meten is, vaak te beïnvloeden is, en tegelijk iets zegt over vaten (risicoprofiel) én brein (cognitieve kwetsbaarheid).
Het doel is zelden alleen “een getal omlaag”. Het doel is: de oorzaak vinden en je cardiovasculaire en neurologische belasting verlagen, voordat je klachten krijgt of voordat klachten verergeren.
Wil je weten hoe jouw homocysteïne ervoor staat en wat het voor jou betekent? Neem dan gerust contact met mij op. Dan kijken we samen wat ik voor jou kan betekenen.
Bronnen
[1] Van Binsbergen JJ, Verschuren WMM, Blom HJ. Hyperhomocysteïnemie: opsporen en behandelen? Huisarts & Wetenschap (2002).
[2] Smith AD et al. Homocysteine-lowering by B vitamins slows the rate of accelerated brain atrophy in mild cognitive impairment (VITACOG). PLOS ONE (2010). DOI: 10.1371/journal.pone.0012244
[3] Smith AD et al. Homocysteine and Dementia: An International Consensus Statement. Journal of Alzheimer’s Disease (2018). DOI: 10.3233/JAD-171042
[4] Seshadri S et al. Plasma homocysteine as a risk factor for dementia and Alzheimer’s disease. NEJM (2002). DOI: 10.1056/NEJMoa011613
[5] Lipton SA et al. Neurotoxicity associated with dual actions of homocysteine at the NMDA receptor. PNAS (1997). DOI: 10.1073/pnas.94.11.5923
[6] Lonn E et al. Homocysteine Lowering with Folic Acid and B Vitamins in Vascular Disease (HOPE-2). NEJM (2006). DOI: 10.1056/NEJMoa060900
[7] Bønaa KH et al. Homocysteine lowering and cardiovascular events after acute myocardial infarction (NORVIT). NEJM (2006). DOI: 10.1056/NEJMoa055227
[8] Farmacotherapeutisch Kompas. Vitamine B-groep: waarschuwingen foliumzuur/B12 en pyridoxine.
[9] Lareb. Vitamin B6 and neuropathy (signalering/rapport).
[10] Zhou F et al. Dose-response meta-analysis: homocysteine and Alzheimer-type dementia risk. Clinical Nutrition (2019). DOI: 10.1016/j.clnu.2019.03.022
[11] Jernerén F et al. Brain atrophy in cognitively impaired elderly: the importance of long-chain omega-3 fatty acids and B vitamin status in a randomized controlled trial. Am J Clin Nutr (2015). DOI: 10.3945/ajcn.114.103283
[12] Huang T et al. Effect of vitamin B-12 and n-3 fatty acids on plasma homocysteine, ferritin, C-reaction protein, and other cardiovascular risk factors: a randomized controlled trial. Asia Pac J Clin Nutr (2015). DOI: 10.6133/apjcn.2015.24.3.19
[13] Holmes HE et al. Elevated homocysteine is associated with increased rates of epigenetic aging in a population with mild cognitive impairment. Aging Cell (2024). DOI: 10.1111/acel.14255
[14] Vianello E et al. Homocysteine in the Cardiovascular Setting: What to Know, What to Do, and What Not to Do. Biomedicines (2025). DOI: 10.3390/biomedicines13071604
[15] Larsson SC et al. Homocysteine, B vitamins, and cardiovascular disease: a Mendelian randomization study. BMC Medicine (2021). DOI: 10.1186/s12916-021-01977-8
[16] Miller JW et al. Concerning the debate about homocysteine, B vitamins, and dementia. J Alzheimers Dis (2025). DOI: 10.1177/13872877251350297
[17] Zuliani G et al. High plasma homocysteine levels predict the progression from mild cognitive impairment to dementia. Exp Gerontol (2024). DOI: 10.1016/j.exger.2024.112456